Con la llegada de los coches, motos, bicis, trenes y en general medios de transporte propulsados por pilas de combustible de hidrógeno se ha tendido a instaurar la idea de que tan solo existe un tipo de pilas de combustible, y no, nada más lejos de la realidad. Una pila de combustible es básicamente un convertidor electroquímico en el que tienen lugar sendas reacciones electroquímicas de forma separada. Sobre un electrodo (ánodo) se lleva a cabo la oxidación de un combustible con lo que se generan una serie de electrones que circulan por un circuito externo. En el otro electrodo (cátodo) tiene lugar de forma independiente al anterior una reacción de reducción, de forma que el oxidante capta los electrones procedentes del circuito externo. Además, para que el sistema pueda funcionar de forma continuada tiene que tener lugar un tránsito de iones entre ambos electrodos a través de un electrolito que lo permita. Este electrolito a su vez debe impedir el flujo de electrones en su interior, porque sino no se podría establecer un flujo externo de electrones, y nos habríamos cargado el invento. Viendo este principio de funcionamiento, en el que no aparece la palabra hidrógeno en ningún sitio, se llega a la conclusión de que pueden existir multitud de tipos de pilas de combustible. Por ejemplo en función del tipo de combustible utilizado o en función del tipo de catalizador empleado. Pero es que incluso dentro de aquellas que emplean hidrógeno como combustible surgen diferentes tipos de pilas de combustible en función del electrolito empleado. Hoy vamos a ver brevemente algunas de las formas de clasificar las pilas de combustible.
Pilas de combustible según el combustible utilizado
El hidrógeno es un combustible muy sexy para la gente que trabajamos en esto de la producción de energía eléctrica y pilas de combustible porque tiene una gran densidad energética por unidad de masa, y eso (por lo que sea) nos gusta mucho. Pero claro, el hidrógeno no nos pilla muy a mano. Si te dijese que me trajeses 1 kg de hidrógeno ¿dónde irías a cogerlo? Por poderse, se puede conseguir. Ahora, cuando se requieren cantidades muy grandes ya es otro cantar y si ya se quiere que su producción haya sido no contaminante pues la cosa se complica todavía más. Total, que el hidrógeno es un combustible poco accesible a priori. Además, su almacenamiento tampoco es una cuestión simple (como ya vimos por aquí). Por ello, se han planteado el uso de otros combustibles que son más sencillos de obtener, almacenar y manejar como por ejemplo el metanol, el etanol o la glucosa.
También se estudian otros tipos de combustibles debido a su conveniencia en determinadas situaciones o con la intención de aprovechar posibles fuentes de energía que en otros casos se desperdiciarían. Por ejemplo, el estudio de la glucosa de los fluidos corporales como combustible para pilas de combustible que alimenten dispositivos médicos implantables, el empleo de los desechos humanos para producir electricidad en regiones asoladas por desastres naturales o donde la generación de electricidad es complicada, o el uso de desechos alimenticios como combustible.
Así pues, podemos tener distintas pilas de combustible según el combustible que empleen: de hidrógeno (las más importantes y extendidas), de metanol o etanol (también llamadas pilas de combustible de alcohol directo), de glucosa, biológicas, etc.
Pilas de combustible según el electrolito empleado
Ésta es sin duda la clasificación más conocida y utilizada, la típica que aparece en los manuales y que es la que aquí voy a exponer hace referencia al hidrógeno aunque se puede extrapolar fácilmente a otros combustibles si es necesario. Cinco son los tipos de pilas de combustible según esta clasificación:
-
Pilas de combustible con membranas alcalinas como electrolito (PEM):
También denominadas pilas de combustible con membrana de intercambio de protones ( Polymer Electrolyte Membrane o Proton Exchange Membrane)
- Electrolito: membranas poliméricas conductoras de protones. La marca más conocida y utilizada de este tipo de membranas es Nafion de las casa DuPont.
- Carga en movimiento: H+
- Catalizadores típicos: Pt depositado sobre un sustrato carbonoso. También puede ser Pt-Ru si los reactantes contienen trazas de CO o CO2.
- Temperatura de funcionamiento: 60 – 80 ºC (Baja temperatura)
-
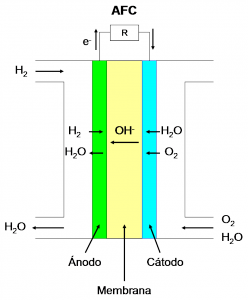
Pilas de combustible alcalinas (AFC, Alkaline Fuel Cells):
- Electrolito: una base fuerte, habitualmente KOH, que es retenida en una matriz tradicionalmente de asbesto.
- Cargas en movimiento: OH–
- Catalizadores típicos: muy diversos, níquel, plata, platino, oro, óxidos metálicos, etc.
- Temperatura de funcionamiento:
- Baja temperatura (<120 ºC) en este caso se suele emplear una baja concentración de la base fuerte (30 – 50% en peso)
- Alta temperatura (~ 250 ºC) en este caso se carga bien la matriz con base fuerte (~85% en peso).
-
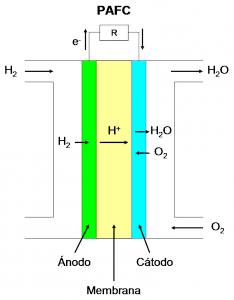
Pilas de combustible de ácido fosfórico (PAFC, Phosphoric Acid Fuel Cells):
- Electrolito: pues con este nombre no pueden utilizar otra cosa que ácido fosfórico y bien concentrado eh, sin tonterías, en torno al 100%. Igual que en las AFC se utiliza una matriz para retener el electrolito, en este caso suele ser de SiC.
- Cargas en movimiento: H+
- Catalizadores típicos: Pt
- Temperatura de funcionamiento: unos 220 ºC
-
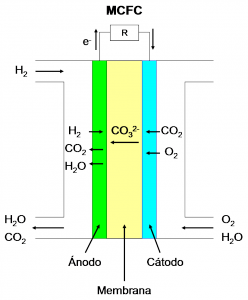
Pilas de combustible de carbonatos fundidos (MCFC, Molten Carbonate Fuel Cells):
- Electrolito: carbonatos alcalinos embebidos en una matriz cerámica.
- Cargas en movimiento: CO32-
- Catalizadores típicos: metales no nobles (Ni con Cr o Al, u óxidos metálicos). No son necesarios metales nobles porque a estas temperaturas las cinéticas de reacción mejoran notablemente.
- Temperatura de funcionamiento: 600 – 700 ºC, a estas temperaturas los carbonatos forman una sal fundida con una gran conductividad iónica.
-
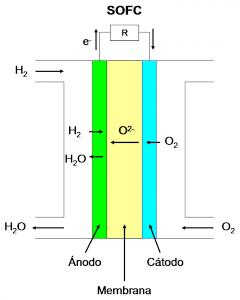
Pilas de combustible de óxido sólido (SOFC, Solid Oxide Fuel Cells):
- Electrolito: óxido metálico, típicamente Y2O3 estabilizado con óxido de circonio (YSZ).
- Cargas en movimiento: O2-
- Catalizadores típicos: níquel junto con compuestos cerámicos en el ánodo y lantano estroncio manganita (LSM) en el cátodo. Igual que en las MCFC dadas las elevadas temperaturas, no es necesario emplear metales nobles para acelerar las reacciones electroquímicas.
- Temperatura de operación: 600 – 1000 ºC, a estas temperaturas se produce una gran conductividad iónica del electrolito gracias a la movilidad de los aniones oxígeno.
|
Tipo de pila de combustible |
Cargas en movimiento | Temperaturas de operación |
| PEMFC |
H+ |
60 – 80 ºC |
| AFC |
OH– |
50 – 250 ºC |
| PAFC |
H+ |
150 – 220 ºC |
| MCFC |
CO32- |
600 – 700 ºC |
|
SOFC |
O2- |
600 – 1000 ºC |
Pilas de combustible según los catalizadores empleados
Puede decirse que esta clasificación es bastante reciente. Hace años, lo habitual y prácticamente la única opción que se estudiaba eran los electrodos metálicos, ya fuese platino u otros elementos como plata, níquel o paladio y sus aleaciones. Sin embargo, hoy en día con los avances de la biología están surgiendo y se están estudiando nuevos tipos de catalizadores, sobre todo orientados a aumentar la velocidad de las reacciones de oxidación de combustibles orgánicos, como son las enzimas o las colonias de microorganismos. Con estos catalizadores se puede por un lado mejorar la oxidación de los compuestos orgánicos (producir más electrones por molécula de combustible) y por otro aumentar la vida de los electrodos. Evidentemente, también presentan sus retos particulares como por ejemplo anclar los compuestos catalíticos a un electrodo de forma eficiente para facilitar el trasvase de los electrones de las enzimas al electrodo, o aumentar la vida de estos compuestos y retardar su desnaturalización para aumentar la durabilidad de las pilas de combustible.
Pilas de combustible según el método de suministro de los reactantes
En función de cómo los reactantes se suministren a la pila de combustible esta puede ser activa o pasiva.
- Activas: existen dispositivos externos a la pila de combustible, bombas o compresores, que suministran los reactantes y eliminan los productos. Es decir, los reactantes se suministran mediante un proceso convectivo (diferencia de presiones) a los electrodos.
- Pasivas: las pilas de combustible pasivas totales no requieren dispositivos auxiliares de suministro, en su lugar emplean la difusión por diferencia de concentración para suministrar los reactantes y eliminar los productos. Estas pilas de combustible presentan un menor peso que las anteriores, sin embargo, dado que los reactantes alcanzan los puntos catalíticos de los electrodos solo por difusión las densidades de potencia que son capaces de ofrecer son muy inferiores. Con hidrógeno este tipo de pilas de combustible pueden ser complicadas de construir, pero con combustibles líquidos como el metanol es bastante simple. Se pone un depósito con metanol que esté en contacto con el o los ánodos y los cátodos se dejan al aire para que en ellos reaccione el oxígeno del aire y listo.
Ahora bien, es posible que en una pila de combustible haya un electrodo activo y otro pasivo por ejemplo. Y luego ya puedes hacerte mezclas muy locas en plan una pila de combustible de metanol con membrana alcalina, enzimas como catalizadores en el ánodo activo y platino-rutenio como catalizador en el cátodo pasivo.
Hay muchos tipos de pilas de combustible y muchas clasificaciones (o taxonomías como dirían los biólogos) posibles según diferentes criterios. La realidad es que cada vez se amplía más el abanico para tratar de dar soluciones a los diversos problemas que se plantean. Las clasificaciones son un mero artificio para tratar de entender rápidamente cada tipo de pila de combustible y los fenómenos que en ella tienen lugar, pero lo realmente importante es el principio de funcionamiento que hemos descrito más arriba. Esa es la esencia de las pilas de combustible, la cuestión es jugar con el resto de elementos respetando los principios de la electroquímica para que el dispositivo funcione. Por ejemplo, unas pilas de combustible con las que trabajo solo presentan una entrada, es decir, no se suministra el combustible al ánodo y el oxidante al cátodo por separado sino que ambos reactantes están en una misma solución y se difunden por una única abertura, y para colmo no tienen membrana porque la solución hace también de electrolito. Esta pila no cuadra en casi ninguna de las clasificaciones mostradas anteriormente, pero sin embargo, se ha jugado con los diferentes elementos hasta conseguir que la pila de combustible funcione.
Hay mucha gente investigando más allá de las pilas de combustible de hidrógeno de tipo PEM, no te olvides de ellos, ellos no lo harían ;).
Quizás te interese:
3 métodos para el almacenamiento de hidrógeno





Gracias, buen trabajo. 🙂
Combustible Sexy!!! o.O lo ultimo
Es muy interesante todo lo que aqui explican,gracias.
Hola buenas, estoy haciendo un proyecto sobre el tema y me interesaría saber el precio que tienen las pilas, o donde podría encontrarlo.
Gracias.